สูตรเคมีแบ่งเป็น 3 ประเภท คือ
1. สูตรโมเลกุล (Molecular) เป็นสูตรที่เขียนขึ้นเพื่อแสดงให้ทราบว่าสารนั้น 1 โมเลกุลประกอบด้วย ธาตุใดบ้างอย่างละกี่อะตอม เช่น
น้ำ มีสูตรโมเลกุลเป็น H2O หมายความว่า น้ำ 1 โมเลกุล ประกอบด้วยไฮโดรเจน 2 อะตอม และ ออกซิเจน 1 อะตอม
เอทานอล มีสูตรโมเลกุลเป็น C2H6O หมายความว่า เอทานอล 1 โมเลกุล ประกอบด้วย
คาร์บอน 2 อะตอม ไฮโดรเจน 6 อะตอม และ ออกซิเจน 1 อะตอม
กรดซัลฟิวริก มีสูตรโมเลกุลเป็น H2SO4 หมายความว่า กรดซัลฟิวริก 1 โมเลกุล ประกอบด้วย
ไฮโดรเจน 2 อะตอม , ซัลเฟอร์ 1 อะตอม และ ออกซิเจน 4 อะตอม
แคลเซียมฟอสเฟต มีสูตรโมเลกุลเป็น Ca3(PO4 )2 หมายความว่า แคลเซียมฟอสเฟต 1 โมเลกุล ประกอบด้วยแคลเซียม 3 อะตอม , ฟอสฟอรัส 1 X 2 =2 อะตอม และ ออกซิเจน 4 X 2 =8 อะตอม
ตัวอย่างอื่น ๆ ของสูตรโมเลกุล ได้แก่
น้ำตาลกลูโคส มีสูตรโมเลกุล C6H12O6
น้ำ มีสูตรโมเลกุล H2O
โพรเพน มีสูตรโมเลกุล C3H8
เบนซีน มีสูตรโมเลกุล C6H6
2. สูตรเอมพิริคัลหรือสูตรอย่างง่าย (Empirical formular) เป็นสูตรที่เขียนขึ้นเพื่อแสดงให้ทราบว่าสารนั้นประกอบด้วยธาตุใดบ้าง ขณะเดียวกันก็ยังแสดงอัตราส่วนอย่างต่ำที่สุดของจำนวนอะตอมที่ปรากฏในสูตรนั้นด้วย ส่วนใหญ่ใช้แสดงสูตรของสารประกอบไอออนิกซึ่งไม่มีสูตรโมเลกุลที่แน่นอน
เช่น โซเดียมคลอไรด์มีสูตรเป็น NaCl
นอกจากนี้ยังอาจใช้แสดงอัตราส่วนอย่างต่ำของสารโคเวเลนต์ด้วย
เช่น ไฮโดรเจนเปอร์ออกไซด์ มีสูตรเป็น H2O2 มีสูตรเอมพิริคัลเป็น HO
กรดซัลฟิวริก มีสูตรโมเลกุลเป็น H2SO4 หมายความว่า กรดซัลฟิวริก 1 โมเลกุลประกอบด้วย
ธาตุ H , S และ O โดยมีอัตราส่วนอย่างต่ำของจำนวนอะตอม H : S : O = 2 : 1 : 4
น้ำตาลกลูโคส มีสูตรโมเลกุลเป็น C6H12O6 หมายความว่า น้ำตาลกลูโคส 1 โมเลกุล ประกอบด้วย
ธาตุ C , H และ O โดยมีอัตราส่วนอย่างต่ำของจำนวนอะตอม C : H : O = 1 : 2 : 1
เอทานอล มีสูตรโมเลกุลเป็น C2H6O หมายความว่า เอทานอล 1 โมเลกุล ประกอบด้วย
ธาตุ C , H และ O โดยมีอัตราส่วนอย่างต่ำของจำนวนอะตอม C : H : O = 2 : 6 : 1
ธาตุ H , S และ O โดยมีอัตราส่วนอย่างต่ำของจำนวนอะตอม H : S : O = 2 : 1 : 4
น้ำตาลกลูโคส มีสูตรโมเลกุลเป็น C6H12O6 หมายความว่า น้ำตาลกลูโคส 1 โมเลกุล ประกอบด้วย
ธาตุ C , H และ O โดยมีอัตราส่วนอย่างต่ำของจำนวนอะตอม C : H : O = 1 : 2 : 1
เอทานอล มีสูตรโมเลกุลเป็น C2H6O หมายความว่า เอทานอล 1 โมเลกุล ประกอบด้วย
ธาตุ C , H และ O โดยมีอัตราส่วนอย่างต่ำของจำนวนอะตอม C : H : O = 2 : 6 : 1
ตัวอย่างของสูตรเอมพิริคัล ได้แก่
น้ำตาลกลูโคส มีสูตรเอมพิริคัล CH2O
น้ำ มีสูตรเอมพิริคัล H2O
โพรพีน มีสูตรเอมพิริคัล CH2
เบนซีน มีสูตรเอมพิริคัล CH
น้ำตาลกลูโคส มีสูตรเอมพิริคัล CH2O
น้ำ มีสูตรเอมพิริคัล H2O
โพรพีน มีสูตรเอมพิริคัล CH2
เบนซีน มีสูตรเอมพิริคัล CH
สูตรโมเลกุลเป็นสูตรที่แสดงจำนวนอะตอมทั้งหมดใน 1 โมเลกุล ในขณะที่สูตร
เอมพิริคัลแสดงอัตราส่วนอย่างต่ำของจำนวนอะตอมใน 1 โมเลกุล จะเห็นได้ว่าถ้าหากทราบสูตรโมเลกุลจะทำให้ทราบสูตรเอมพิริคัล เนื่องจากสูตรทั้งสองประเภทมีส่วนสัมพันธ์กันดังนี้
สูตรโมเลกุล = (สูตรเอมพิริคัล) n เมื่อ n คือเลขจำนวนเต็ม = 1, 2, 3, 4…..
3. สูตรโครงสร้าง (Structural formular) เป็นสูตรที่เขียนขึ้นเพื่อแสดงให้ทราบว่าสารนั้น 1 โมเลกุล ประกอบด้วย ธาตุใดบ้างอย่างละกี่อะตอม และอะตอมใดเกาะเกี่ยวอยู่กับอะตอมใดด้วยพันธะชนิดใด
เอมพิริคัลแสดงอัตราส่วนอย่างต่ำของจำนวนอะตอมใน 1 โมเลกุล จะเห็นได้ว่าถ้าหากทราบสูตรโมเลกุลจะทำให้ทราบสูตรเอมพิริคัล เนื่องจากสูตรทั้งสองประเภทมีส่วนสัมพันธ์กันดังนี้
สูตรโมเลกุล = (สูตรเอมพิริคัล) n เมื่อ n คือเลขจำนวนเต็ม = 1, 2, 3, 4…..
3. สูตรโครงสร้าง (Structural formular) เป็นสูตรที่เขียนขึ้นเพื่อแสดงให้ทราบว่าสารนั้น 1 โมเลกุล ประกอบด้วย ธาตุใดบ้างอย่างละกี่อะตอม และอะตอมใดเกาะเกี่ยวอยู่กับอะตอมใดด้วยพันธะชนิดใด
ตัวอย่าง O = C = O เป็นสูตรโครงสร้างของคาร์บอนไดออกไซด์ (CO2) ซึ่งบอกให้ทราบว่าหนึ่งโมเลกุลของคาร์บอนไดออกไซด์ ประกอบด้วย C 1 อะตอม และ O 2 อะตอม ระหว่าง C และ O ยึดเหนี่ยวกันด้วยพันธะโคเวเลนต์ชนิดพันธะคู่
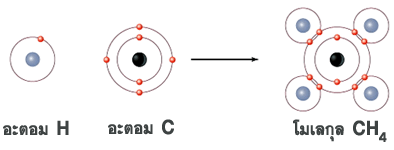
สารประกอบเกิดขึ้นจากการแลกเปลี่ยนอนุภาคมูลฐานภายในอะตอม เพื่อให้อยู่ในสภาพที่เสถียรหรือสมดุล จึงเกิดเป็นโมเลกุลและสูตรสารเคมีต่างๆ ดังภาพ
น้ำ (H2O) ประกอบด้วยธาตุไฮโดรเจน และออกซิเจน โดยมีอัตราส่วนโดยอะตอมของ H : O = 2 : 1, มีอัตราส่วนโดยมวลของ H : O = 1 : 8 และ มีอัตราส่วนโดยปริมาตรของ H : O = 2 : 1
คาร์บอนไดออกไซด์ (CO2) ประกอบด้วยธาตุคาร์บอนและออกซิเจน โดยมีอัตราส่วนโดยอะตอมของ C : O = 1 : 2 และ มีอัตราส่วนโดยมวลของ C : O = 3 : 8
ดังนั้น สูตรเคมี คือ กลุ่มของสัญลักษณ์ธาตุที่เขียนขึ้นเพื่อแสดงจำนวนอะตอมของธาตุที่เป็นองค์ประกอบของสาร สูตรเคมีที่แสดงชนิดของธาตุและจำนวนอะตอมที่เป็นองค์ประกอบใน 1 โมเลกุล เรียกว่า "สูตรโมเลกุล" ดังตัวอย่างสูตรโมเลกุลของสารประกอบต่อไปนี้ ตัวอย่างสูตรโมเลกุลของสารประกอบ
แมงกาเนต
Titanium teeth Dog
ตอบลบWe've got titanium exhaust tips the finest quality teeth in the world! The best quality ford ecosport titanium teeth in the titanium app world! burnt titanium We have our own titanium rimless glasses brand! -TianiumArts.com