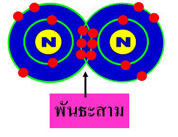
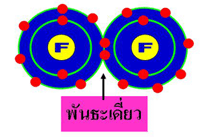
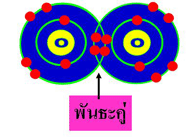
| พันธะโคเวเลนต์ (อังกฤษ: Covalent bond) คือพันธะเคมี ภายใน โมเลกุลลักษณะหนึ่ง พันธะโคเวเลนต์เกิดจากอะตอมสองอะตอมใช้ เวเลนซ์อิเล็กตรอนหนึ่งคู่หรือมากกว่าร่วมกัน ทำให้เกิดแรงดึงดูดที่ รวมอะตอมเป็นโมเลกุลขึ้น อะตอมมักสร้างพันธะโคเวเลนต์เพื่อเติมวง โคจรอิเล็กตรอนรอบนอกสุดให้เต็ม ดังนั้น อะตอมที่สร้างพันธะโคเวเลนต์ จึงมักมีเวเลนซ์อิเล็กตรอนอยู่มาก เช่น ธาตุหมู่ VI และหมู่ VII เป็นต้น พันธะโคเวเลนต์แข็งแรงกว่าพันธะไฮโดรเจนและมีความแข็งแรงพอ ๆ กับพันธะไอออนิกพันธะโคเวเลนต์มักเกิดขึ้นระหว่างอะตอมที่มีค่า อิเล็กโตรเนกาทิวิตีใกล้เคียงกัน ธาตุอโลหะมีแนวโน้มที่จะสร้างพันธะ โคเวเลนต์มากกว่าธาตุโลหะซึ่งมักสร้างพันธะโลหะ เนื่องจากอิเล็กตรอน ของธาตุโลหะสามารถเคลื่อนอย่างอิสระ ในทางกลับกัน อิเล็กตรอนของ ธาตุอโลหะไม่สามารถเคลื่อนที่ได้อย่างอิสระนัก การใช้อิเล็กตรอนร่วมกัน จึงเป็นทางเลือกเดียวในการสร้างพันธะกับธาตุที่มีสมบัติคล้าย ๆ กัน อย่างไรก็ดี พันธะโคเวเลนต์ที่มีโลหะนั้นมีความสำคัญอย่างยิ่งใน การเร่งปฏิกิริยา ตัวอย่างเช่น พันธะโคเวเลนต์ระหว่างสารอินทรีย์กับ โลหะเป็นเครื่องมือสำคัญของกระบวนการสร้างพอลิเมอร์หลายๆ กระบวนการ เป็นต้นอย่างไรก็ตาม ในการศึกษาในระดับที่สูงขึ้นจะพบว่า พันธะ โคเวเลนต์ไม่จำเป็นต้องเกิดขึ้นระหว่างธาตุโลหะกับอโลหะเท่านั้น |
"บริเวณที่มีความหนาแน่นสัมพัทธ์ของอิเล็กตรอนสูงระหว่างนิวเคลียส ที่มีการใช้อิเล็กตรอนร่วมกันและก่อให้เกิดแรงดึงดูดและระยะทางระหว่างนิวเคลียสที่เป็นเอกลักษณ์เฉพาะ"
ไม่มีความคิดเห็น:
แสดงความคิดเห็น